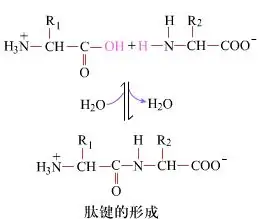
In superficie, formatio vinculis peptidis, dipeptidis cedentibus, est processus chemicus simplex.Hoc significat duo amino acidi, vinculo peptide, vinculo amido, cum dehydrato coniunguntur.
Formatio vinculi peptide est activatio amino acidi sub condiciones reactionis lenis.(A) medietas carboxyl, acidum amino secundum (B) medietas nucleophilica reducitur carboxyl tunc dipeptidem format (AB)."Si pars carboxyl non servatur, formatio vinculi peptidis coerceri non potest."Per-producta ut peptides lineares et cyclicas cum compositis AB componi possunt.Omnes igitur coetus functiones functiones non implicatae in formatione vinculi peptidis custodiendae sunt, modo convertitur tempore peptidis synthesis.
Itaque, synthesis peptide - formatio cuiusque vinculi peptidis - tres gradus aggregationis involvit.
Primus gradus est aliqua amino acida praeparare quae praesidio indigent et structura zwitteronica amino acida non iam exstat.
Secundus gradus est duplicatus reactionem ad vincula peptida formare, in qua globus carboxyl amino acido N-tutus primum ad medium activum reducitur et postea vinculum peptide formatur.Haec reactio copulata fieri potest vel sicut unus gradus reactionis vel sicut duae motus sequentes.
Tertius gradus est amotio selectiva seu plenaria amotionis basi tutelae.Etsi omnis amotio nonnisi fieri potest, postquam omnes vincula peptide congregata sunt, electiva amotio coetuum tutelaris requiritur etiam ad synthesin peptida continuandam.
Quia 10 amino acida (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, Sua, Sec et Cys) continent partes catenae functionis lateralis, quae tutelam selectivam requirunt, synthesin peptida magis implicata faciunt.Bases tutelae temporalis et semi-perpetuae distinguendae sunt propter varias requisitas ad selectivity.Sodalitates tutelae temporariae proximo gradu adhibentur ad tutelam amino acidi vel carboxyl functionis temporalis reflectendam.Sodalitates semi-permanentes tutelae tolluntur sine impedimento vincula peptide formato vel amino acidi enotatum, interdum in synthesi.
« Specimen, activatio componentis carboxyl ac subsequentis formationis vinculorum peptidum (coniunctionum reactiones) debet esse celeri, sine formatione racemico vel producto, ac reactante molares applicari ad alta commoda consequenda.Dolendum est, nullae methodi chemicae copulationis his requisitis satisfacere, et paucae ad synthesim practicam idoneae sunt.
In synthesi peptide, coetus functionis in variis reactionibus implicatas plerumque cum centro manuali coniungi solent, glycine excepta sola exceptio et periculum rotationis potentiale est.
Ultimus gradus in synthesi cycli peptide est remotio omnium coetuum tutelaris.Selectiva remotio coetuum tutelaris magni momenti est ad extensionem catenae peptidis, praeter exigentiam plenam remotionem tutelae in synthesi dipeptidi.Consilia synthetica diligenter pertractanda sunt.Secundum opportuna electione N potest selective removere α-amino vel carboxylo coetus protegens.Terminus "strategy" refertur ad ordinem motus condensationis singulorum amino acidarum.Differunt generatim inter synthesim gradalem et condensationem fragmenti.Synthesis peptide (etiam quae "synthesin conventionalis") fit in solutione.In pluribus, gradatim extensio catenae peptidis nonnisi componi potest, utendo catena peptide ad fragmenta breviora componenda.Ad syntheses longiores peptidas, moleculae scopo in fragmenta convenientia divisa esse debent et determinari ut gradum differentiae in termino C minuere possint.Postquam singula fragmenta paulatim convenerunt, scopo composito coniungetur.Consilium synthesis peptidis involvit electionem fragmenti optimi et aptissimi tutelae, et consilium synthesis peptidis includit electio aptissima compositionis basium tutelaris et optima methodus fragmenti coniugationis.
Post tempus: Iul-19-2023